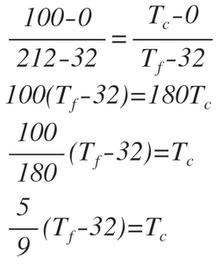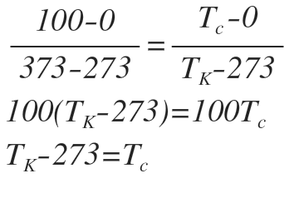LA TERMODINÁMICA.
Ahora conviene dirigir la atención al estudio de la termodinámica, que abarca situaciones en que la temperatura o el estado (sólido, líquido o gas) de un sistema cambian debido a transferencias de energía. Como aprenderá, la termodinámica es muy conveniente para explicar las propiedades volumétricas de la materia y la correlación entre estas propiedades y los mecanismos de átomos y moléculas. El desarrollo histórico de la termodinámica fue paralelo al de la teoría atómica de la materia. Hacia 1820 los experimentos químicos habían proporcionado evidencia contundente de la existencia de los átomos. En aquella época, los científicos reconocieron que entre la termodinámica y la estructura de la materia debía existir una conexión. En 1827, el botánico Robert Brown reportó que granos de polen suspendidos en un líquido se movían erráticamente de un lugar a otro como si estuvieran bajo agitación constante. En 1905, Albert Einstein usó la teoría cinética para explicar la causa de este movimiento errático, conocido en la actualidad como movimiento browniano. Einstein explicó este fenómeno al suponer que los granos están bajo bombardeo constante de moléculas “invisibles” en el líquido, y que son éstas las que se mueven erráticamente. Esta explicación dio luz a los científicos acerca del concepto de movimiento molecular y proporcionó credibilidad a la idea de que la materia está hecha de átomos. En estos términos se forjó una conexión entre el mundo cotidiano y los bloques constructores invisibles que conforman este mundo. La termodinámica también aborda cuestiones más prácticas. ¿Alguna vez se ha preguntado cómo un refrigerador es capaz de enfriar su contenido, o qué tipos de transformaciones se presentan en una planta eléctrica o en el motor de su automóvil, o qué ocurre con la energía cinética de un objeto en movimiento cuando llega al reposo? Es posible aplicar las leyes de la termodinámica para proporcionar explicaciones de éstos y otros fenómenos (Serway tomo I, p.531).
TEMPERATURA Y LEY CERO
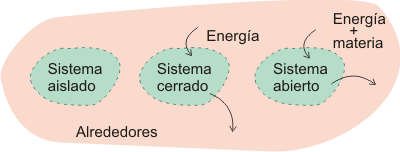
Sistemas termodinámicos Sistema: cualquier grupo de átomos, moléculas, partículas u objetos en estudio termodinámico. Por ejemplo el agua dentro de un envase, el cuerpo de un ser vivo o la atmósfera.
Ambiente o Alrededor: todo lo que no pertenece al sistema, es lo que rodea al sistema, sus alrededores. Por ejemplo el exterior al envase donde está el agua, o el espacio que rodea a la atmósfera (puede ser todo el Universo). Entre el sistema y el ambiente puede haber intercambio de calor y de energía y se puede realizar trabajo.
Sistema cerrado: sistema en el cual no entra ni sale masa, pero que puede intercambiar calor y energía con el ambiente.
Sistema abierto: sistema que puede tener variación de masa, como por ejemplo intercambio de gases o líquidos, o de alimentos en los seres vivos.
Sistema cerrado aislado: sistema en el cual no se produce ningún intercambio de calor o energía con el ambiente a través de sus fronteras
Ambiente o Alrededor: todo lo que no pertenece al sistema, es lo que rodea al sistema, sus alrededores. Por ejemplo el exterior al envase donde está el agua, o el espacio que rodea a la atmósfera (puede ser todo el Universo). Entre el sistema y el ambiente puede haber intercambio de calor y de energía y se puede realizar trabajo.
Sistema cerrado: sistema en el cual no entra ni sale masa, pero que puede intercambiar calor y energía con el ambiente.
Sistema abierto: sistema que puede tener variación de masa, como por ejemplo intercambio de gases o líquidos, o de alimentos en los seres vivos.
Sistema cerrado aislado: sistema en el cual no se produce ningún intercambio de calor o energía con el ambiente a través de sus fronteras
Magnitudes físicas
Cada sistema se puede caracterizar mediante variables que determinan su estado, la relación de estas variables determinará alguna función matemática que permitirá determinar el estado futuro o pasado del sistema termodinámico.
Las variables pueden ser extensivas como la energía interna, la entro pía, el volumen, composición molar....cuyo valor depende de la masa o tamaño del cuerpo y son aditivas. Por lo general el cociente de dos magnitudes extensivas da como resultados una intensiva como es el caso de la densidad = masa / volumen.
Las magnitudes intensivas son aquellas que no dependen de la cantidad masa como la temperatura, la presión, la velocidad, el volumen específico, la densidad...
Las variables pueden ser extensivas como la energía interna, la entro pía, el volumen, composición molar....cuyo valor depende de la masa o tamaño del cuerpo y son aditivas. Por lo general el cociente de dos magnitudes extensivas da como resultados una intensiva como es el caso de la densidad = masa / volumen.
Las magnitudes intensivas son aquellas que no dependen de la cantidad masa como la temperatura, la presión, la velocidad, el volumen específico, la densidad...
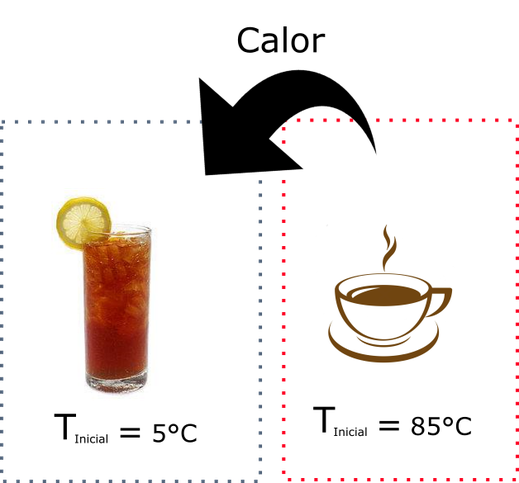
Temperatura, calor y ley ceroMuchas veces en la vida cotidiana usamos temperatura y calor de manera indistinta para referirnos a ciertos fenómenos, pero debemos físicamente, hacer una distinción en aquello, pues calor y temperatura son dos conceptos distintos que están relacionados, pero la temperatura no es la medida del calor como muchas veces se piensa, como tampoco el calor no es una característica del sistema, sino una relación entre dos o más cuando están a diferente temperatura. Por ello el calor lo entenderemos como una energía en tránsito que se produce cuando dos o más sistemas termodinámicos tienen distinta temperatura, lo anterior se efectuará hasta que todos los sistemas involucrados alcances la misma temperatura, es decir, el equilibrio térmico.
En la imagen anterior se observa que hay dos sistemas termodinámicos con distinta temperatura inicial. Suponiendo que alrededor de ellos no hay ningún otro sistema, entonces entre ambos habrá un flujo de calor Q, una energía en tránsito, produciendo después de un tiempo que la temperatura en ambos sea igual. Este punto se denomina equilibrio térmico (ver siguiente figura).
|
Ley cero de la termodinámicaLa ley cero de la termodinámica fue formulada por primera vez en el año 1931 por Ralph Fowler. T
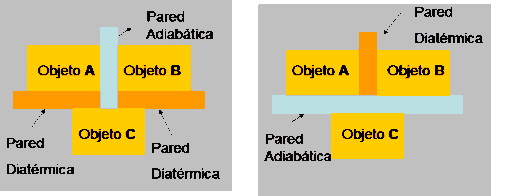
Se puede enunciar así la ley cero: "Cuando dos sistemas A y B se encuentran por separado y en equilibrio térmico con un tercer sistema C, se dice que A y B están en equilibrio térmico uno del otro". En la imagen de la izquierda se observa que el cuerpo A está en equilibrio con C, pero el objeto A y B están aislado. También se observa que el cuerpo C está en equilibrio con B. Finalmente se concluye que A y B están en equilibrio térmico.
En la imagen del lado derecho, la pared adiabática se colocado de manera horizontal, luego podemos decir que A y B están en equilibrio térmico, pero no podemos decir que C lo esté con A y/o con B. La ley cero es lo que ocurre con la medición de la temperatura con un termómetro. El termómetro es un buen ejemplo de aplicación de la ley cero de la termodinámica, pues al medir por ejemplo la temperatura de un vaso de agua, el agua está en contacto con el vidrio y el vidrio con el mercurio, luego el mercurio de dilata o contrae según corresponda midiendo la temperatura según en la escala que esté graduado. Así el agua está en equilibrio térmico con el vidrio, y el vidrio con el mercurio, luego el mercurio y el agua están a la misma temperatura.
|
Escalas de temperatura
La temperatura desde un punto de vista microscópico es una medida de la energía cinética promedio de las partículas del sistema. Esta energía cinética considera la energía cinética de rotación, vibración y traslación de las moléculas. Para mayor profundización véase teoría cinética de los gases.
Las escalas de temperatura están basada en referencias a fenómeno físico a condiciones estándar (1 atm de presión y con g=9,8 m/s^2 ) que se le asigna un número determinado.
Nombre de la Escala Punto de referencia Números asociados
Transfusión del agua 0°C
Ebullición del agua 100°C
Absoluta o Kelvin Está construida tomando como referencia la temperatura más baja teórica que se puede alcanzar, y que para la fusión y ebullición del agua corresponde respectivamente 273 y 373
Fahrenheit La temperatura más baja ocurrida durante el invierno de 1708-1709 en la ciudad de Dazing, ahora llamada Gdansk en Polonia, cerca de -17,8 ºC0
Temperatura del cuerpo humano ante una ligero estado febril 100La temperatura desde un punto de vista microscópico es una medida de la energía cinética promedio de las partículas del sistema. Esta energía cinética considera la energía cinética de rotación, vibración y traslación de las moléculas. Para mayor profundización véase teoría cinética de los gases.
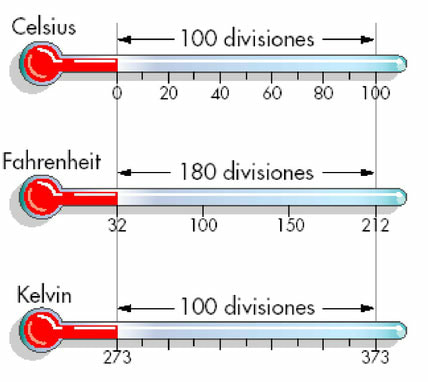
Las escalas de temperatura están basada en un fenómeno físico que por comodidad ha sido la temperatura del punto equilibrio entre hielo y vapor de agua saturado a presión atmosférica normal (punto de congelación) y el punto de equilibrio entre agua liquida y su vapor a presión de 1atm (punto de ebullición). En la escala Celsius asignó respectivamente el número 0 y 100, mientras que en la escala Fahrenheit estos puntos son 212 y 32, y en la escala absoluta 273,15 y 373,15 respectivamente.-
Uno de los termómetros usados para definir escalas de temperatura es el termómetro de gas a volumen constante (TGVC) siguiendo los pasos:
Las escalas de temperatura están basada en referencias a fenómeno físico a condiciones estándar (1 atm de presión y con g=9,8 m/s^2 ) que se le asigna un número determinado.
Nombre de la Escala Punto de referencia Números asociados
Transfusión del agua 0°C
Ebullición del agua 100°C
Absoluta o Kelvin Está construida tomando como referencia la temperatura más baja teórica que se puede alcanzar, y que para la fusión y ebullición del agua corresponde respectivamente 273 y 373
Fahrenheit La temperatura más baja ocurrida durante el invierno de 1708-1709 en la ciudad de Dazing, ahora llamada Gdansk en Polonia, cerca de -17,8 ºC0
Temperatura del cuerpo humano ante una ligero estado febril 100La temperatura desde un punto de vista microscópico es una medida de la energía cinética promedio de las partículas del sistema. Esta energía cinética considera la energía cinética de rotación, vibración y traslación de las moléculas. Para mayor profundización véase teoría cinética de los gases.
Las escalas de temperatura están basada en un fenómeno físico que por comodidad ha sido la temperatura del punto equilibrio entre hielo y vapor de agua saturado a presión atmosférica normal (punto de congelación) y el punto de equilibrio entre agua liquida y su vapor a presión de 1atm (punto de ebullición). En la escala Celsius asignó respectivamente el número 0 y 100, mientras que en la escala Fahrenheit estos puntos son 212 y 32, y en la escala absoluta 273,15 y 373,15 respectivamente.-
Uno de los termómetros usados para definir escalas de temperatura es el termómetro de gas a volumen constante (TGVC) siguiendo los pasos:
- Se recopilan las lecturas de presión para el punto de congelación y ebullición del agua.
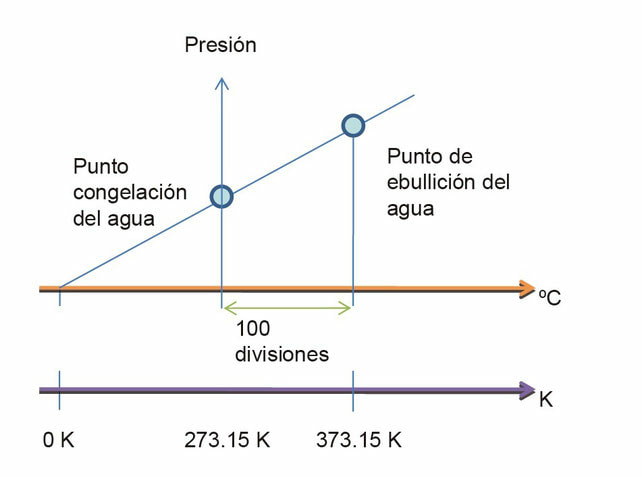
- Se dividen estas lecturas en 100 porciones, se le asigna 0 al punto de congelación y 100 al punto de ebullición. Esta es la llamada escala CELSIUS.
- Sin embargo, tiene mas sentido dejar el cero en la escala de temperatura cuando la presión tiende a ser cero. Por lo tanto se puede extrapolar el cero en P, este seráel punto donde la temperatura es cero. Esto funciona si es que el volumen se mantiene constante. Luego el punto de congelación del agua es de 273.15 divisiones desde el cero y el punto de ebullición 373.15 divisiones desde el cero.
Transformación de escalasLa imagen de la derecha muestra la divisiones para las tres escalas de temperatura más usadas. Vamos a encontrar una ecuación para transformar de grados Celsius a Fahrenheit, para ello procedemos de la siguiente manera:
|
Siguiendo el mismo razonamiento podemos encontrar la equivalencia entre Celcius y Kelvin y entre cualquier escala que queramos siguiendo el mismo procedimiento. Se deja al lector la tarea de encontrar una ecuación para convertir de Fahrenheit a Kelvin
|
videos
|
|
|